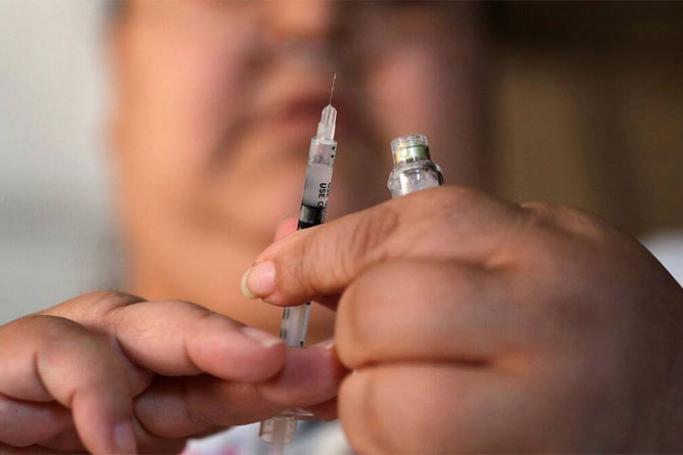
အိန္ဒိယနိုင်ငံ ပူနေးမြို့အခြေစိုက် Gennova Biopharmaceuticals Ltd ကုမ္ပဏီက ထုတ်လုပ်သည့် နိုင်ငံ၏ ပထမဆုံး mRNA ကိုဗစ်-၁၉ ကာကွယ်ဆေးသည် ဘေးအန္တရာယ်ကင်းရှင်းကြောင်း တွေ့ရှိရသဖြင့် အဆင့် ၂ နှင့် ၃ စမ်းသပ်မှုများကို ဆက်လက်လုပ်ဆောင်ရန် အိန္ဒိယ ဆေးဝါးထိန်းချုပ်ရေးရေးအဖွဲ့ (DCGI) က ခွင့်ပြုလိုက်သည်။
အဆင့် ၁ စမ်းသပ်မှုမှ တွေ့ရှိချက်များကို ကုမ္ပဏီက အိန္ဒိယအစိုးရ၏ နိုင်ငံတော် စည်းကမ်းထိန်းချုပ်ရေး အာဏာပိုင်အဖွဲ့၏ ဗဟိုဆေးဝါးစံနှုန်းထိန်းချုပ်ရေးလုပ်ငန်းသို့ တင်ပြခဲ့ခြင်းဖြစ်သည်။
“HGCO190 ဆေး ပထမအဆင့် စမ်းသပ်မှုကို ပူနေးမှာ ၂ နေရာနဲ့ ကိုဟာပါ ၁ နေရာတို့မှာ လူ ၈၂ ဦးကို စမ်းသပ် အောင်မြင်ခဲ့ပါတယ်။ လုံလောက်တဲ့ ဘေးကင်းလုံခြုံမှုကို တွေ့ရလို့ အဆင့် ၂ နဲ့ ၃ စမ်းသပ်မှုတွေ ဆက်လုပ်ဖို့ ခွင့်ပြုချက်ရခဲ့ပါတယ်။ နောက် ၂ ပတ်အတွင်းမှာ ဆက်လုပ်သွားပါမယ်” ဟု Gennova Biopharmaceuticals Ltd ဆေးကုမ္ပဏီ၏ အမှုဆောင်အရာရှိချုပ် ဒေါက်တာဆန်ဂျေး ဆင်းဂ်က The Indian Express သို့ ပြောကြားခဲ့သည်။
အဆင့် ၂ အတွက် စမ်းသပ်မှုကို နေရာပေါင်း ၁၀ မှ ၁၅ နေရာခန့်နှင့် အဆင့် ၃ အတွက် နေရာ ၂၂ မှ ၂၇ နေရာအထိ လုပ်ဆောင်သွားဖွယ်ရှိသည်။ ယင်းစမ်းသပ်မှုများအတွက် ဇီဝနည်းပညာဌာန၏ အိန္ဒိယဆေးသုတသနကောင်စီ၏ စမ်းသပ်ကုသမှု ကွန်ရက်ကို အသုံးပြုရန် စီစဉ်ထားသည်။
“လာမယ့် စမ်းသပ်မှုတွေမှာ လူပေါင်း ၄၄၀၀ အထိ ပါဝင်မယ်လို့ မျှော်လင့်ထားပါတယ်” ဟု ဒေါက်တာဆင်းဂ်က ပြောသည်။
“ဒီဆေးကို အတတ်နိုင်ဆုံး ဒီနှစ်မကုန်မီ ထုတ်ဖို့ မျှော်လင့်ထားပါတယ်။ အရွယ်ရောက်သူတွေအတွက် အသုံးပြုပြီးရင် ကလေးတွေအတွက်လည်း ဆက်လက်ထုတ်ပါမယ်” ဟု ၎င်းကပြောကြားသည်။
Gennova ကုမ္ပဏီ၏ mRNA အခြေခံ ကိုဗစ်ကာကွယ်ဆေး ထုတ်လုပ်သည့်အစီအစဉ်ကို ဇီဝနည်းပညာဌာနက တစ်စိတ်တစ်ပိုင်း ပံ့ပိုးထားခြင်းဖြစ်သည်။